作为食物咀嚼的主要器官,牙齿由表面外胚层来源上皮和神经嵴衍生的外胚间充质组织间相互作用形成,是研究上皮和间质相互作用的经典组织器官发育模型之一。同时,牙胚上皮细胞和间充质细胞可通过自组装再生整颗牙齿,表明在牙胚中可能存在具有牙齿诱导能力的关键干细胞群,而这一关键细胞群及其分子特征至今未知。因此,干细胞介导的全牙再生仍面临巨大挑战。

2022年12月6日,beat365李中瀚教授、田卫东教授、蔡浩洋教授的研究团队在Cell Reports上发表题为“Dental niche cells directly contribute to tooth reconstitution and morphogenesis”的研究论文。该研究通过单细胞测序,利用生物信息学技术,表征了从胚胎到出生后阶段(E12.5到PN7)磨牙发育过程中上皮细胞和间充质细胞的细胞动态变化,并结合DistMap方法高精度表征了在E14.5磨牙表达的基因位置。其中Sdc1被鉴定为牙乳头的特异性标记,而牙龛细胞表达其他特征基因。令人惊讶的是,体外牙胚重建和体内肾被膜移植结果显示牙龛细胞表现出比Msx1+Sdc1+牙乳头更强的牙齿诱导能力,并形成了成簇的牙齿,同时也表明Msx1+Sdc1+牙乳头细胞可以直接从牙上皮和牙齿牙龛细胞之间的相互作用中再生。在此基础上,研究人员进一步从牙龛细胞中鉴定了一组以前未被鉴定的Msx1+Sox9+细胞可能是牙乳头的细胞起源,在发育过程中迁移并取代了原始的牙原基。综合上述,该研究表结果表明牙龛细胞直接参与了牙齿的器官发育,可以为进一步开发牙齿生物工程重建新技术提供重要理论支撑。
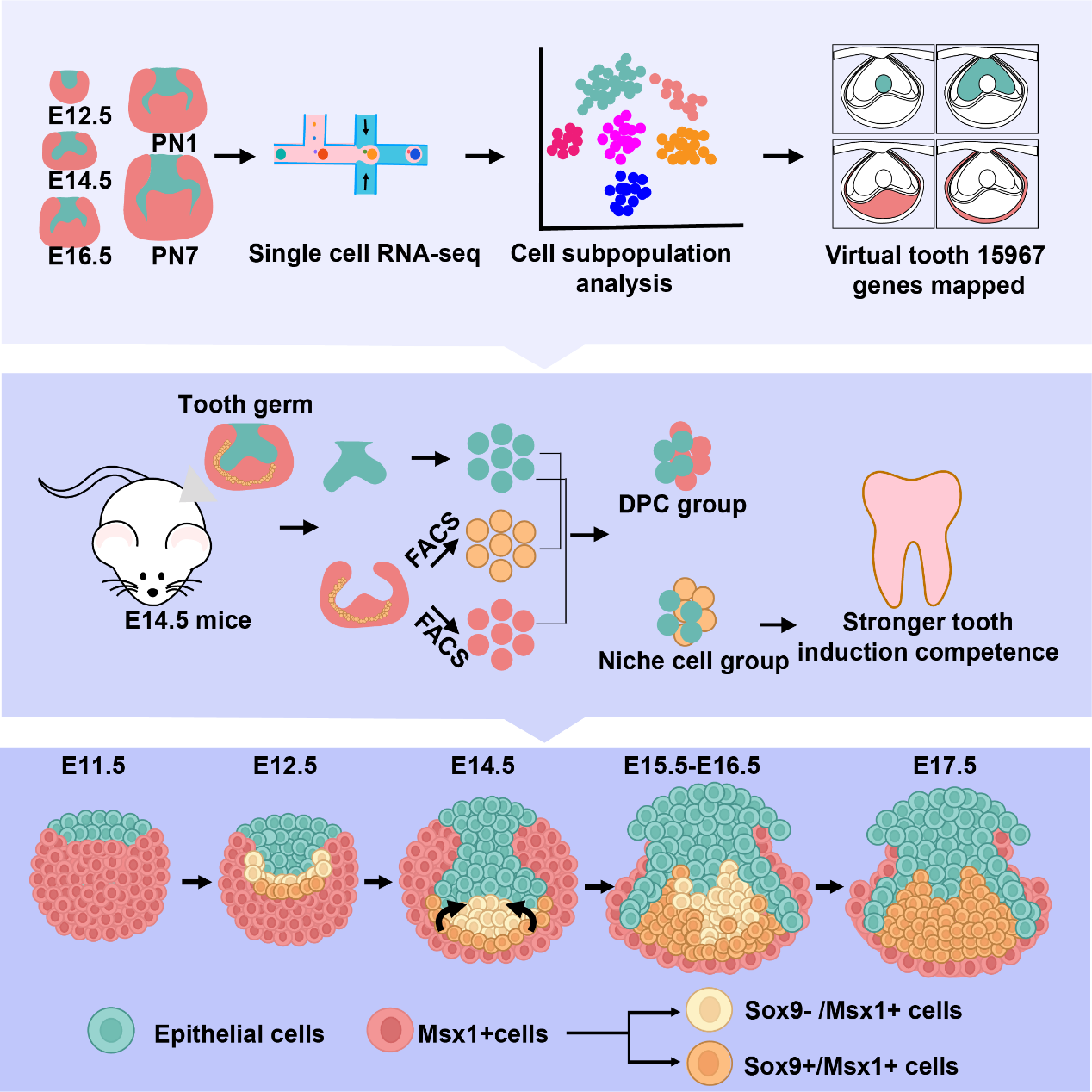
首先,研究者构建了一个双荧光小鼠模型来跟踪和分析牙上皮和间质,通过免疫荧光染色对小鼠E12.5-PN7的牙胚进行染色,发现Pitx2-copGFP和Msx1-tdTomato可以分别标记不同发育阶段的牙上皮和间质组织。通过重建牙胚进一步确认了胚胎期Pitx2+上皮细胞和Msx1+间质细胞含有牙齿重组再生的所有必要细胞群。研究者们随后对牙胚上皮和间充质单独进行单细胞转录组测序,通过拟时序分析,发现上皮细胞以线性轨迹排列而间充质细胞表现出多个分支,表明在磨牙发育过程中经历了多种细胞命运分化。通过DistMap进行空间映射,研究者对E14.5的表达在牙胚中的15967基因进行了空间定位,有效地恢复了每个细胞群的空间信息并鉴定了具有特异性表达谱的基因。利用免疫荧光或荧光原位杂交进一步证实了Sdc1和Enpp1在发育中的牙乳头中特异性富集而C1qtnf3、Cdkn1c和Postn等在牙龛细胞中特异性表达。研究者借助虚拟牙齿模型,更清晰、更准确地描述了牙胚基因的空间分布与动态变化。
随后,研究者们聚焦E14.5时期的牙胚进行了深入分析,将牙间充质细胞分为两群细胞,即牙乳头细胞群和牙龛细胞群,其中牙乳头细胞群用Sdc1/Enpp1进行标记。分选重组实验结果显示 牙龛细胞较牙乳头细胞而言具有更强的牙齿重组再生能力,并且牙龛细胞群与上皮重组后,在发育过程中能够产生牙乳头细胞,说明牙龛细胞具有诱导并发育为一个完整牙齿的潜能。同时,为了研究牙龛细胞如何促进牙齿形成,研究者们在体外建立了牙胚类器官培养系统。通过牙胚类器官培养,发现牙龛细胞促进了牙齿上皮的重组和存活,并且再次证明牙龛细胞和上皮之间的相互作用可以直接再生牙乳头细胞。总的来说,体内移植的重组牙胚和体外的牙胚类器官均证实牙龛细胞包含与牙齿上皮相互作用并有效诱导牙齿重建的关键干细胞群。
在此基础上,研究者进一步探究了牙龛细胞群的亚群组成与相互间关系。拟时序分析显示牙龛细胞确实比牙乳头前体处于更早的祖细胞状态,且通过不同时期的免疫荧光染色显示Msx1+Sox9+细胞首先在E12.5的牙龛中被观察到,随后包围着牙乳头。从E15.5~16.5开始,这些细胞开始侵入牙乳头区域,并成为主要群体。因此,Msx1+Sox9+牙龛细胞可能代表了一组以前未被鉴定的牙胚祖细胞,在牙齿形态发生过程中迁移并取代了原始原基。随后,研究者使用Sox9 IRES-CreERT2小鼠和LSL-tdTomato小鼠进行体内谱系示踪研究,不同时期的标记与示踪观察发现,从Sox9+牙龛细胞的确参与了牙胚发育过程,从 E16.5开始迁入牙乳头区域,并逐渐成为牙乳头主体。随后,利用Sox9-EGFP小鼠牙龛细胞进行牙胚体外重组也进一步确认了,仅有Sox9+牙龛细胞具备牙胚重组能力。综上所述,这些研究证明了牙龛细胞确实直接参与了牙胚发育与重组再生,是人工构建完整牙胚的关键细胞亚群。
在本研究中,beat365博士生胡红、段余峰、王琨、付换成作为该论文的共同第一作者,beat365李中瀚教授、田卫东教授、蔡浩洋研究员作为该论文的共同通讯作者。该研究获得了科技部重点研发计划“干细胞研究与器官修复”和“干细胞及转化研究”项目、国家自然科学基金、国家特聘计划青年项目、beat365理科原创基金等的资助。
原文链接:
http://doi.org/10.1016/j.celrep.2022.111737
